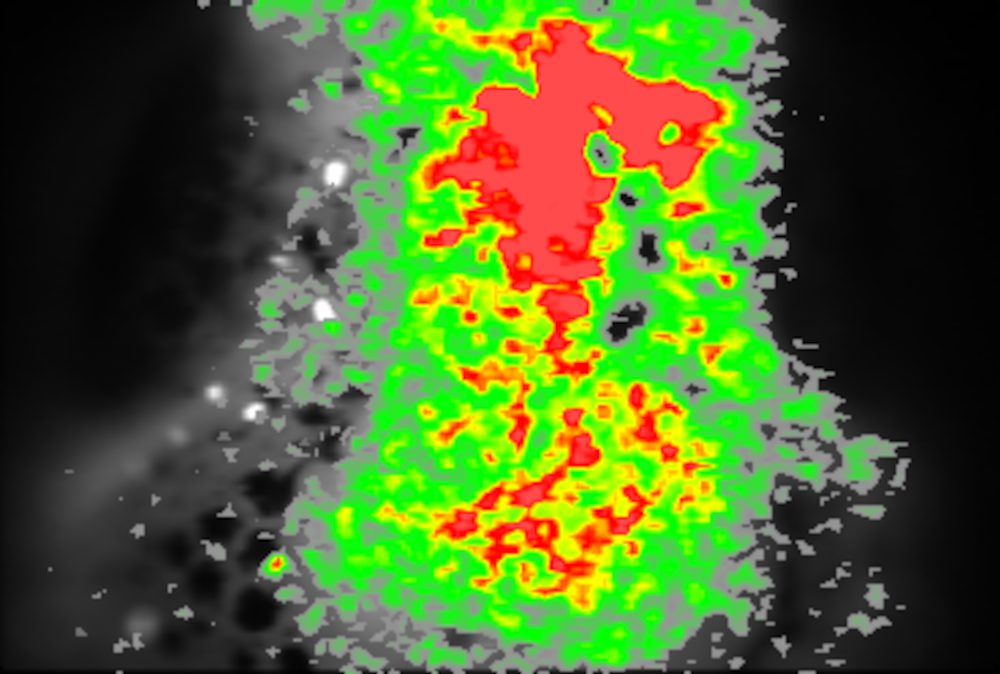
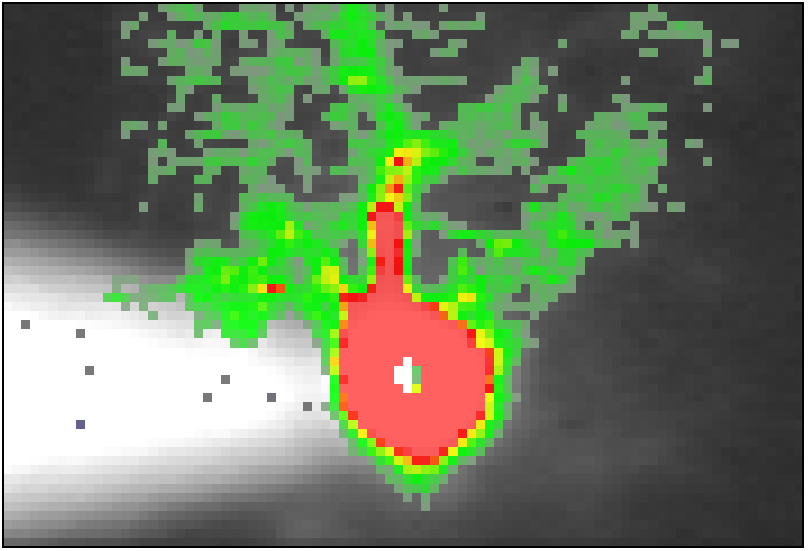
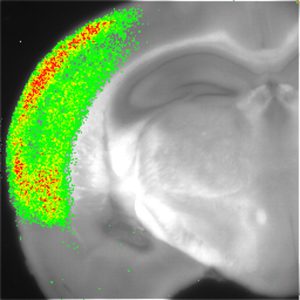
カルシウム指示薬の種類とカルシウムイメージングへの応用
カルシウムイオンは細胞内で重要な役割を果たしており、その動態を正確に測定することは、細胞生物学や神経科学の研究において極めて重要です。
しかし、どの試薬を選ぶべきか迷っている方も多いでしょう。
カルシウム指示薬には、Fura-2、Fluo-4、Rhod-2など、さまざまな種類があります。それぞれの試薬は異なる波長特性や解離定数を持っているため、特定の研究目的や実験条件に応じて使い分ける必要があります。
本記事では、カルシウムイメージングに使用されるさまざまな試薬の種類と選び方について解説します。
目次
カルシウム指示薬の定義
カルシウム指示薬は、細胞内のカルシウムイオン(Ca²⁺)の濃度を測定するために使用される化学物質です。蛍光カルシウム色素、カルシウム感受性色素などとも呼ばれます。
カルシウムイオンは、筋収縮や神経伝達などの生理的プロセスにおいて重要な役割を果たしています。カルシウム指示薬は、カルシウムイオンと結合すると蛍光を発する性質を持つため、これによりカルシウムの濃度変化を視覚的に確認することができます。
カルシウム指示薬の種類
カルシウム指示薬には以下のような種類があります。
(1)カルシウムキレート剤を利用したカルシウム感受性蛍光色素
EGTAやBAPTAなどのCa²⁺選択的キレート試薬を用いたカルシウム感受性蛍光色素。1980年にR. Y. Tsienにより開発されたQuin-2/AMを始めとして、Fura-2、Fluo-3、Indo-1、Rhod-2など様々な種類のものが開発された。
(2) エクオリンなどのカルシウム感受性発光タンパク質
Ca2+と結合すると微弱な光を出す発光タンパク質であるエクオリンを利用。
(3) CameleonやGCaMPなどの遺伝子でコードされたカルシウム感受性蛍光タンパク質
Ca²⁺結合性のカルモジュリンを利用した蛍光タンパク質。
本ページではカルシウム感受性蛍光色素に絞ってその原理や種類について説明します。
カルシウム指示薬の動作原理
カルシウム指示薬は主にキレート剤と蛍光体が結合したものです。Ca²⁺が指示薬のキレート部分に結合すると、蛍光特性が変化し、蛍光強度が増加したり蛍光スペクトルが変化します。
BAPTAは、EGTAのメチレン結合がベンゼン環に置き換えられた化合物です。BAPTAは、EGTAに匹敵する高いカルシウム選択性を持つが、pH変化の影響が小さく、カルシウムの取り込みと放出がより迅速であるという特徴があります。
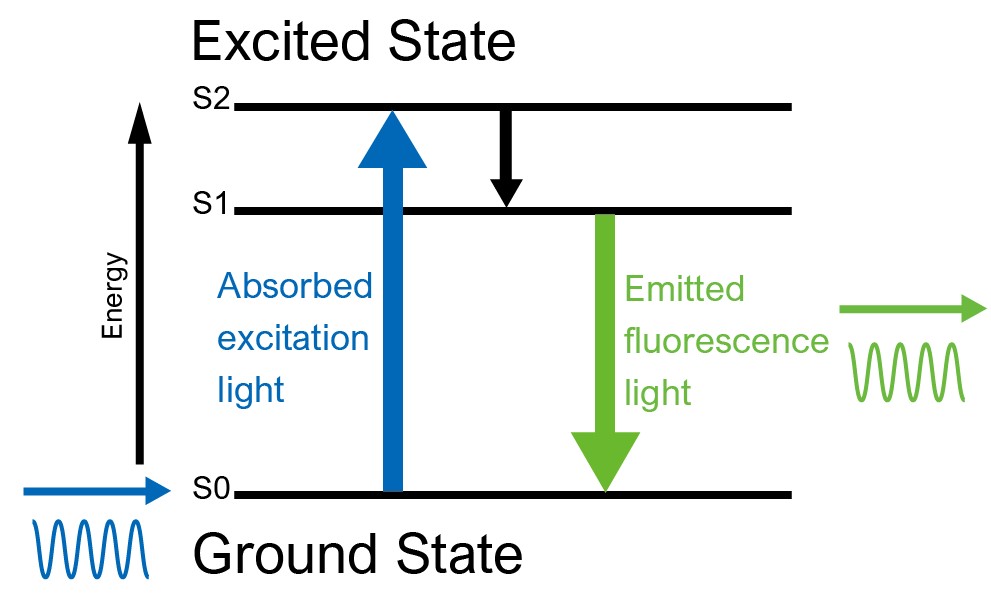
蛍光の発生メカニズム
蛍光物質は特定の波長の光を吸収します。この光エネルギーは、蛍光物質内の電子を基底状態から励起状態へと引き上げます。
吸収されたエネルギーにより、電子は高エネルギーの励起状態に移動します。この状態は不安定であり、電子はすぐにエネルギーを失って基底状態に戻ります。
電子が基底状態に戻るときに、吸収した光エネルギーの一部を光として放出します。この放出される光は、吸収された光よりも長い波長、つまり低いエネルギーを持つことが一般的です。この現象はストークスシフトとして知られています
放出された光は、蛍光として観察されます。蛍光の波長と強度は、蛍光物質の特性や周囲の環境条件に依存します。最も効率よくこれらの遷移を起こす波長が極大励起波長と極大蛍光波長となります。
カルシウム指示薬の種類
カルシウム指示薬にはさまざまな種類があります。大きく分けて蛍光指示薬と吸収指示薬の2種類がありますが、現在吸収タイプはあまり使用されていません。
さらに蛍光タイプは、(1)イオン濃度変化に応じて蛍光強度が変化するものと(2)イオン濃度変化に応じて励起あるいは蛍光スペクトラムが変化するものに分けられます。
(1)イオン濃度変化に応じて蛍光強度が変化
(1-1) 1波長励起1波長蛍光 (例: Fluo-3, Fluo-4、Rhod-2など)
特徴
蛍光強度の変化から相対的なカルシウム濃度の変化の情報を得ることができる。一般的に、測定開始時の蛍光強度に比べてどれだけ変化したか、その変化率(ΔF/F)で表される。
メリット
- 2波長測定のように波長を変えて測定する必要がないため測定が簡単
- ほとんどが可視光励起のため、紫外線透過の光学系を必要とせず、細胞に対する光障害も少ない。
デメリット
蛍光色素の濃度の違いや分布のムラがあったり、細胞の厚みが変化する場合、あるいは強い励起光により蛍光の退色(bleaching)が激しい時には、正確なCa²⁺イオン濃度変化の測定が困難になる。
(2)イオン濃度変化に応じて励起あるいは蛍光スペクトルが変化
(2-1) 2波長励起1波長蛍光 (例:Fura-2)
(2-2) 1波長励起2波長蛍光 (例:Indo-1)
特徴
励起波長あるいは蛍光波長として2波長を使用する。
メリット
- 2波長の蛍光強度の比をとることにより、イオン強度の変化とは無関係な蛍光強度の変動(濃度の違いや細胞の厚みの変化など)を補正できる。
- 適当なキャリブレーションを行えば、イオン濃度の絶対値を求めることができる。
デメリット
- 2波長を使用して測定するための特殊な光源や波長を分岐する装置が必要
- 紫外線を使用するため、紫外線を透過する光学系が必要。また細胞に対する光障害が大きい。
主なカルシウム指示薬の一覧:高親和性
主なカルシウム指示薬の一覧:低親和性
| 試薬名 | 励起波長 (nm) | 蛍光波長 (nm) | 解離定数 (Kd) | 備考 | メーカーのURL |
|---|---|---|---|---|---|
| Fluo-4FF AM | 494 | 516 | 9.7μM | single wavelength | https://www.thermofisher.com/order/catalog/product/F23981 |
| Fluo-5N AM | 494 | 516 | 90μM | single wavelength | https://www.thermofisher.com/order/catalog/product/F14204 |
| Rhod-5N | 551 | 576 | 320μM | single wavelength | https://www.thermofisher.com/order/catalog/product/R14207 |
どのカルシウム感受性蛍光色素を選べば良いか?
- 細胞毒性がないこと
- 測定しようとするCa²⁺濃度変化に比べて十分に速い反応速度を有すること
- Ca²⁺に対する親和性(Kd値)が生理的な値に近いこと
- 励起光が細胞を障害しないこと
- 顕微鏡の光路特性に試薬の励起波長・蛍光波長が合致していること
- 他のイオンにより妨害が少ないこと
細胞への導入
蛍光プローブ試薬を測定対象の細胞内に導入しなければならないのですが、水溶性のためそのままでは細胞膜を透過できないません。そこで細胞膜の透過性が高くなるように修飾した試薬を用いたり、試薬を直接細胞内に注入する方法がとられます。
- マイクロインジェクション
- エステラーゼ活性が低い細胞で利用される
- 細胞内へ微小電極を刺入
- パッチピペットからの灌流
- エステラーゼ活性が低い細胞で利用される
- 脂溶性エステルによる導入
- プローブ試薬にAcetoxymethyl(AM)基をエステル結合させて脂溶性としたAM誘導体がよく使われる。AM誘導体そのものは無蛍光で、遊離イオンとは結合能力がない。
- 細胞膜を透過しやすいため、AM誘導体を含んだ液に細胞を浸しておくと細胞外のイオンと結びつくことなしに細胞膜を透過して細胞内に入る。プローブ試薬が細胞内に入るとAM基はエステラーゼにより切り離され、イオンとの結合能を獲得する。また、水溶液となるため生体膜を透過できるようになり細胞質内にとどまる。プローブの導入が困難な組織塊標本では界面活性剤(Cremophore EL)を用いるとうまくいく場合もある。
サンプルデータ