2. 計測の問題点―ノイズと信号
ブレインビジョン株式会社 市川道教
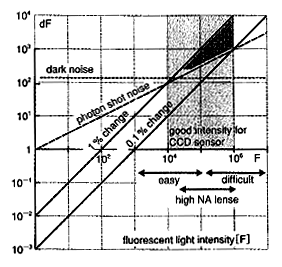
前項で述べたように、この手法は非常に有用であり、それほど難しい技術でもない。しかしながら、多くの知識とノウハウがなければ十分な計測結果は得られない。たとえば、ノイズを小さくしたいのであれば、光を明るくすれば当然よい。しかし、強烈な照明は、色素の変性と試料のダメージを誘起して、結果として正しい計測が果たせないのである。膜電位感受性色素を用いた計測で良い結果を得るには、いかに照明を抑え、いかに染色を抑え、それでいて、いかに明るい映像を捉えることを可能にするか、という問題にこたえることである。当然、そこには大いなる努力に基づいた妥協が必要である。まず、ノイズと信号、光強度の関係を図3に示したので参照してほしい。この図の横軸は色素の発する蛍光の総量で、縦軸は蛍光の変化成分であり、どちらも対数軸である。数値はわれわれの用いているセンサーの1個のピクセル(約35μm角)に露光される光の光量子数である。2本の45度の黒の実線は、神経の活動によって代表的な膜電位感受性色素(Di4-ANEPPS)が変化する信号を示し、上が1%のラインで、下が0.1%のラインである。試料によって信号の大きさにはバリエーションがあるが、多くの場合、0.2%とか、0.6%といった値になり、この2本の直線の間に入る。計測装置自身がもっているノイズは一般に光量とは無関係なので、赤の点線で示したような水平な直線になる。これより、暗い領域の観察はほとんど無理であるが、多くの場合、このラインを超えるのは容易である。実際上、最も問題となるノイズは、赤の破線で示した光量の平方根で増加する光ショットノイズである。光ショットノイズは、光の粒子性(光子)に基づく雑音であり、物理的にさけようがないノイズである。このラインの上ならば、信号がノイズを上回り、S/N比は1以上ということになる。図中*で示した領域が、実質的にS/N=1程度の領域である。当然、これより右の明るい領域ならば、より良いS/N比で計測が可能である。
ところが、問題はそのような明るい光学系(蛍光顕微鏡)が存在しないことである。明るくするためには照明を強くすることになるが、試料に対するダメージが大きくなる。ごく一般的な蛍光顕微鏡などで得られる蛍光量は、図3右下のeasyという矢印が示す範囲で、特別に開口率の高いレンズを工夫した場合に、high NAの矢印で示す蛍光量が実現できる。それより、明るいものは現状では存在せず、明るくするためには照明の光源を強くする以外にない。普通、100~150Wのハロゲン電球を光源に用いるが、500W級の光源に変更しても、3~5倍程度の輝度向上であり、S/Nの改善は平方根なのでせいぜい2倍程度である。ところが、試料のダメージは照明に対し線形かそれ以上に悪化するので、経験的に10倍程度は悪化する。つまり、2倍の改善を10倍の犠牲で得ることになる。もちろん、1回だけでも高いS/N比で観察ができれば目的を達成できるという実験ならば、躊躇なく強烈な光源を用意すべきだろう。しかし、多くの場合は、長時間安定な計測を前提にした実験の組み立てになるのも事実である。
図3 光計測の信号量とノイズの検討図
以上のように、膜電位感受性色素の変化が、1%以下であるという事実が変わらない限り、S/N比は向上できないという問題は認めざるをえない。これを克服するには、①明るいレンズ系を使う、②最も信号が大きく、最もダメージの少ない染色方法を見出す、③データ処理によって、ノイズを除去する、という努力が必要である。このうち、②は実験者自身の努力が大きく、実験的に見つけ出すこと(コラム参照)になるが、①と③は、装置の開発によって達成することができる。そして、最も大切なのは、何が見たいのかを明確にし、その計測プロトコールを十分に検討することである。たとえば、非同期の現象を観察したいのでアベレージングができないという場合がある。しかし、なんらかの同期信号を取り出す別の計測(たとえば、細胞外電極)を同時記録し、その信号に対して同期をかけることが可能でないか検討することは非常に価値がある。もし、可能ならアベレージングでS/N比は大幅に改善できるのである。
| 経験的に見出された有効な染色法 | |
| ① | Di4-ANEPPS(5mg)のビンに、1mlのアルコールを直接入れて、よく溶解する。 (カタログにはメタノールとあるが、エタノールの方がよく溶ける) |
| ② | そこに、クレモフォア-EL10%水溶液を0.5ml加えて、よく溶解してストック液とする。冷蔵庫で2~3か月は保存可能。 |
| ③ | 上記のストック液35μmを0.5ml仔ウシ血清と0.5mlのACSFに溶かして、染色液にする。最終濃度は約0.1mg/mlである。 |
| ④ | スライスは、インターフェースチェンバーのような状態を保つことができる密閉型の染色容器を作り、上記の染色液をスライスの表面に少量ずつ滴下して、約20分間静置する。温度は室温、容器内部でACSFを5%二酸化炭素・酸素ガスをパブリングして、酸素と湿気を保つ。 |
| ⑤ | スライスを観察チェンバー(サブマージュ型、顕微鏡の下に設置)に運び、約30分間インキュベートしてから観察に入る。 この方法で、約4時間程度は安定な観察ができる。 |
(出典 共立出版 「光による医学診断」(2001年3月30日出版))
3. 明るい光学系と高速カメラシステム >